|
DISCUSIÓN ANATOMO CLÍNICA
Paciente de 26 años
trasplantado de médula ósea. Resultado de una autopsia
parcial
Reunión
Anatomoclínica realizada el 16/09/2009
Discutidor invitado: Luciano Salvano (Clínica Reina Fabiola)
Servicio de Patología: Bürgesser, María Virginia – Diller,
Ana
Servicio de Clínica Médica: Garzón, María Isabel –
Amuchástegui, Tomás – Caeiro, Enrique
Servicio de
Diagnóstico por imágenes: Orozco, Santiago
Hospital Privado Centro Médico de Córdoba
Revista Facultad de Ciencias
Medicas 2011; 68(1):33-38
Autor para
correspondencia:
Bürgesser, María Virginia
Dirección: Naciones Unidas 346. Barrio Parque Vélez
Sarsfield. Córdoba, Argentina. CP: X5016KEH; Teléfono:
0351-4688829; Fax: 0351-4688826
Email:
virburgesser@gmail.com
Historia Clínica
Paciente de 26 años de edad ingresó al hospital por diarrea
de 10 días de evolución. Tenía
antecedentes de Leucemia Linfoblástica Aguda precursora B
diagnosticada en mayo del 2006. En ese momento, recibió
tratamiento de inducción con quimioterapia según protocolo
GATLA 2000. Presentó, como complicación secundaria a
quimioterapia, aspergilosis pulmonar invasiva, que requirió
lobectomía superior de pulmón derecho, insuficiencia
cardíaca con caída de la fracción de eyección, neutropenia
febril, sepsis y requerimiento de cuidados en Unidad de
Cuidados Intensivos (UTI) por cuatro días, con buena
evolución, quedando medicado con voriconazol por un año,
rotándose luego a itraconazol. Sin lograr remisión, se
decidió realizar quimioterapiade reinducción con protocolo
FLAG-Ida.
Una punción de médula ósea posterior
evidenció: remisión hematológica. Se realizó segundo ciclo
de FLAG-Ida. Posteriormente continuó con tratamiento de
mantenimiento con protocolo GATLA 2000 hasta septiembre del
2008. Tres meses posteriores, presentó recaída de la
enfermedad, por lo que recibió FLAG-Ida y reinició
voriconazol. Cursando el día 18 de quimioterapia, presentó
reactivación de aspergilosis pulmonar. Una tomografía axial
computada (TAC) de tórax informó: lesiones fibrocicatrizales
en ambas bases pulmonares, particularmente del lado derecho,
en donde además se objetivó engrosamiento pleural residual.
Se observaron pequeños infiltrados alveolares “acinares” en
campo medio de ambos pulmones y en el superior izquierdo. Un
laboratorio mostró galactomanano (+). Se agregó anfotericina,
con buena respuesta a tratamiento. Sin remisión
hematológica, se decidió realizar ICE,
quedando en aplasia sin evidencia de blastos. Se realizó
trasplante de médula ósea alogénico no relacionado no
mieloablativo, en febrero de 2009. Posterior al trasplante,
presentó como complicación enfermedad injerto versus huésped
(GVH) cutánea e intestinal confirmada por biopsia
intestinal, con insuficiencia renal aguda secundaria, CMV
intestinal, diagnosticado por PCR positivo en tejido, y
negativo en suero plasmático, por lo que inició ganciclovir
endovenoso. Una punción de médula ósea, al día 100
pos-trasplante evidenció: quimerismo 100% donante, ERM (-)
(3).Cursando el día 110 pos trasplante, el paciente ingresó
al hospital por diarrea de 10 días de evolución. Al ingreso
su medicación era: valganciclovir 900mgr. c/12 hs,
espironolactona 25mgr/día, carvedilol 6,25mgr. c/12 hs,
loperamida, tacrolimus, voriconazol 100mgr. c/12 hs, y
enalapril 2,5mgr./dia. Ingresa a sala común. Un laboratorio
informó: Na 142, K1.9,Cl 110, Calcio 8,4,Mg 0.3, Creatinina
1.03 (previa 0,5), urea 36, GB2.900, Hb 11.21,Htc. 32.84,
plaquetas 73.270, FAL 645, LDH 437, PCR 2,GOT 57, GPT 276,
GGT 582, FK-10.1. Recibió metilprednisolona 2 mgr/kgr.
Presentó como complicación otitis media izquierda y
mastoiditis izquierda. Un nuevo laboratorio informó: GB 400,
Hb 8.8, Htc 25, plaquetas 29.100. Recibió múltiples
trasfusiones por pancitopenia progresiva. Permaneció
internado por 23 días, con deterioro progresivo del aparato
respiratorio, con progresión de disnea hasta grado IV,
desaturación y requerimiento de BPAP en sala. Un laboratorio
informó retro y hemocultivo positivos para E. coli BLEE,
galactomanano negativo, GB 1.100, Hb 9.9, Htc 27.8,
plaquetas 20.000, GOT17, GPT 17, GGT 144, FAL 194, LDH 634,
Bil D .20, BilI 0.62, Bil T 1,82., gases:
7.45/35/23.7/0.6/46, ac. láctico 2. Una TAC de tórax
evidenció: extensos infiltrados alveolares en “parches” en
ambos pulmones, algunos en vidrio esmerilado, voluminosas
bullas de enfisema tipo centrolobulillar en ambos lóbulos
superiores, pequeño derrame pleural izquierdo, La
exploración del abdomen superior reveló extensa neumatosis
colónica y neumo-retroperitoneo. Por mala evolución se
decide paso a UTI. Ingresa taquicárdico, taquipneico,
hemodinámicamente inestable, con mala mecánica respiratoria,
con saturación de O2 90% (Fio2 1,0), por lo que
se decide intubación y uso de drogas vasoactivas. Un
laboratorio informó: GB 7.200, Hb 7.4, Htc 22.5, Plaquetas
11.000, gases 7.29/52/24.2/-2.5/79, ac. Láctico 1.6, Na 142,
K5.6, Cl 108. Recibió tratamiento antibiótico con colistin y
tigerciclina, aciclovir, meropenem, y trimetroprima/sulfametoxazol,
como así también múltiples transfusiones. Permaneció en UTI
durante 7 días, con requerimiento de asistencia mecánica
respiratoria desde el ingreso, junto con drogas vasoactivas
sin mejoría. Se constató el óbito del paciente 30 días
después del ingreso.
Presentación y discusión del caso
Dr. Orozco:
En una TAC de tórax de diciembre del 2008 se observan, en el
segmento anterior del lóbulo superior derecho, restos
cicatrizales por una lesión de antigua lobectomía producida
2 años antes. Además se reconocen una pequeña lesión
nodular, otras lesiones de menores dimensiones y pequeño
engrosamiento pleural en la base pulmonar derecha que fueron
interpretadas como de tipo residual.
En febrero de 2009 el paciente, estando en quimioterapia,
presenta fiebre y disnea, realizándose una nueva TAC de
tórax donde se observan infiltrados alveolares, acompañados
de otras lesiones en vidrio esmerilado.
En un control en junio de 2009, el paciente consulta por
diarrea. Se realiza una nueva TAC de tórax, no objetivándose
ningún tipo de lesión significativa.
Luego, el paciente se internó. Pasados 20 días de esta
última internación, el día 23/06, el paciente comienza con
disnea. Se decide hacer una TAC de tórax en inspiración y
espiración. Se puede apreciar que el lóbulo inferior tiene
una densidad un poco mayor que la del segmento del lóbulo
medio. Se reconocen áreas de mayor densidad con áreas de
menor densidad. En las imágenes de los cortes inferiores en
la base del pulmón izquierdo aparecen además, infiltrados
alveolares en parches.
El paciente presentó también un cuadro de otitis por lo cual
se hace una TAC de cráneo. El oído medio y la mastoides
izquierdos se encuentran ocupados por secreción.
Una nueva TAC de tórax en julio de 2009, estando el paciente
internado, muestra infiltrados alveolares en parches,
bastante críticos desde el punto de vista imagenológico.
También, se evidencian infiltrados de tipo alveolar más
consolidativos. En los cortes tomográficos del abdomen
superior se reconoce signo de carácter ominoso que es la
neumatosis colónica.
Dr. Salvano:
Luego del diagnóstico y el tratamiento con quimioterapia, el
paciente, dado el alto riesgo que tenía, tiene indicación de
transplante de médula. El paciente no accede a esa última
indicación y se continúa con el mantenimiento y control.
Hace una recaída en el 2008, al año y medio de recibir el
diagnóstico inicial, por lo cual se vuelve a intentar con la
quimioterapia que había dado resultado. En ese momento, se
reactiva la aspergilosis, con galactomanano positivo y se
trata con anfotericina B. Cuando se repitió esa
quimioterapia, no se logró remisión y no quedaban muchas
opciones efectivas de quimioterapia así que se hizo un
esquema llamado “Ice”, que lleva ifosfamida, carboplatino y
etopósido, que es bastante agresivo también. Se logra
dejarlo sin enfermedad y se le propone un trasplante. El
transplante que se le hace es un transplante no
mieloablativo, que si bien no sería lo ideal, creo que se
podría hacer dadas las comorbilidades del paciente, había
tenido insuficiencia cardiaca, desarrolló aspergilosis, y,
seguramente, la capacidad respiratoria funcional de él
estaba alterada. Entonces se trató de buscar una alternativa
que, con drogas de acondicionamiento, sea lo menos agresiva
posible. Además, este tipo de trasplante tiene la
particularidad favorecer lo que se llama efecto injerto vs.
tumor. Con un tratamiento no mieloablativo, donde la
quimioterapia no es tan intensiva, uno no pretende erradicar
o reafirmar con quimioterapia la desaparición de la
enfermedad pero se busca un efecto inmunológico: que las
células del donante, los linfocitos T hagan una especie de
ataque a la enfermedad que pueda quedar. Esto generalmente
en un transplante no mieloablativo genera el desarrollo de
una enfermedad injerto vs. huésped.
El paciente presentó enfermedad injerto vs. huésped aguda
cutánea e intestinal. Además, presentó una complicación de
infección viral intestinal, lo cual complicó más aún el
cuadro.
A
mí me parece que hay varias patologías. Voy a hablar de las
más probables para mí.
La enfermedad injerto vs. huésped crónica no lo podemos
obviar porque está en el período para hacerlo y el ya había
hecho la forma aguda. Lo que pasa después con el aparato
respiratorio, uno lo podría sospechar como parte de la
enfermedad injerto vs. huésped crónica.
El Aspergilus que tuvo en el año 2006, es muy difícil que se
erradique del todo. Quedó con profilaxis, pero lo volvió a
hacer en la reinducción de quimioterapia. Aunque el
galactomano haya sido negativo al Aspergilus no lo descarta
de ninguna manera.
Desarrolló el citomegalovirus intestinal, que se trató con
aciclovir y tuvo muy buena respuesta pero obviamente debió
quedar con profilaxis con valganciclovir. Estaba con una
profilaxis excelente para eso, pero no da 100 % de seguridad
que no se vaya a reactivar el citomegalovirus, así que es un
cosa en la que yo también pensaría.
Otra cosa que no descartaría es una colitis pseudomembranosa.
Si bien no tenía antibióticos, también se puede presentar en
pacientes neoplásicos con mucha quimioterapia, porque se
altera la flora. Estuvo internado mucho tiempo, puede haber
estado colonizado y en algún momento en que la inmunidad se
alteró, favorecer a que tenga la colitis pseudomembranosa.
Una cosa, que si bien sería rara por la afectación
digestiva, sería neumonía por Pneumocystis jiroveci porque
el paciente está en riesgo de presentarlo a esta altura del
transplante. No estaba con profilaxis por el estado
hematológico.
También podría tratarse de una micobacteriosis.
Le doy mucha relevancia a los siguientes diagnósticos:
enfermedad injerto vs. huésped, infección por
citomegalovirus y aspergilosis pulmonar invasiva.
Dra. Bürgesser:
Como biopsias previas, tenía una de médula ósea en el año
2006 donde se evidencia una infiltración de la misma por
blastos. Es hipercelular y se observan células de escaso
citoplasma, con núcleos redondos y azules. Además están
adosadas unas a otras, correspondiendo a blastos (figura 1).
|
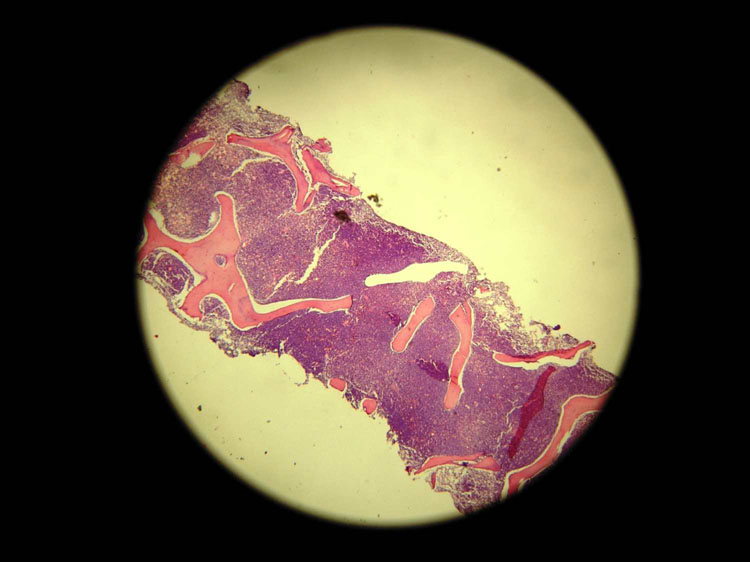 |
Figura 1:
Biopsia de médula
ósea:
Infiltración de médula ósea por
blastos (H/E) |
Posteriormente tiene dos biopsias, un lavado
bronquioalveolar y una biopsia transbronquial donde no se
evidencia patología infecciosa. Al año presenta una nueva
biopsia transbronquial donde no se evidencia patología
infecciosa. Y posteriomente, ante una nueva biopsia
transbronquial, se evidencia un pequeño conglomerado que se
vincula a Aspergillus, por la presencia de estructuras
alargadas, eosinófilas, que se refuerzan con la tinción de
PAS. Por lo tanto, el mismo año se hizo una lobectomía
superior derecha donde se evidenció una cavidad, cuya pared
se encuentra constituida por fibrosis, infiltrado
inflamatorio, necrosis y hemorragia. En su luz se reconocen
polimorfonucleares neutrófilos, fibrina y, con las tinciones
de PAS y metenamina plata, se evidencian mejor estas
estructuras que en parte son redondeadas, algunas alargadas,
que se tabican en 45 º y que son vinculables a Aspergillus
y la lesión cavitada, a un aspergiloma (figura 2).
|
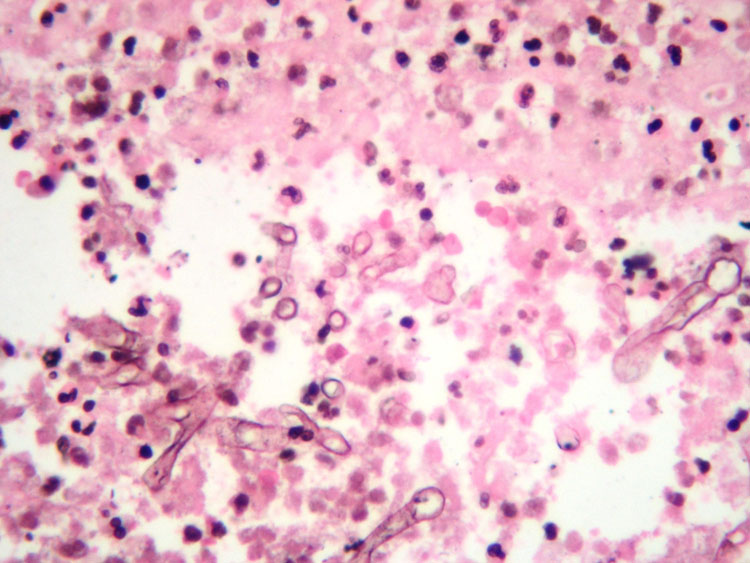 |
Figura 2:
Biopsia de pulmón: Aspergillus en luz
de cavidad pulmonar (Metenamina plata) |
Posteriormente,
en el año 2007 se le hace biopsia de médula ósea donde hay
una hiperplasia mieloide joven, no hay evidencia de
infiltración por blastos pero recae en el año 2008 con nueva
biopsia de médula ósea donde se ve infiltración difusa por
blastos.
Se realizó una biopsia de piel, posterior al transplante de
médula ósea, que evidencia hallazgos vinculables a
enfermedad injerto vs. huésped grado 1. En la misma se ve
epidermis con leve hiperqueratosis, leve fibrosis en la
dermis y a mayor aumento vemos que hay degeneración vacuolar
de la basal, un infiltrado inflamatorio con leucocitos con
exocitosis. Además se evidencian disqueratocitos. Estos
hallazgos se vinculan a enfermedad injerto vs. huésped
cutánea, dentro del contexto clínico.
Finalmente la última biopsia fue de colon, donde se
constatan hallazgos vinculables a enfermedad injerto vs.
huésped grado 1 con edema e inflamación en la lámina propia,
algunos leucocitos migrando en el epitelio glandular y
células apoptóticas. También se reconoce una fisura en
actividad con reepitelización.
En la biopsia de colon no encontramos signos que nos
indicaran efecto citopático viral por citomegalovirus.
La autopsia (nº 8/2009) fue parcial, correspondiendo a un
block cardiopulmonar.
Durante el procedimiento, el pulmón derecho se encontraba
adherido a la pared costal debido a la resección quirúrgica
previa que había tenido. Luego de la fijación del material
en formol, la serosa pleural es de aspecto despulido, tiene
áreas más opacas y la pleura del lado derecho es más
irregular debido a las adherencias a la pared costal. El
hilio pulmonar no presenta evidencias de tromboembolismo
pulmonar y en la luz bronquial se observa contenido hemático.
Al corte, el parénquima pulmonar presenta aspecto
heterogéneo, con moco en las luces bronquiales, áreas de
aspecto hemorrágico y áreas más firmes parduzcas.
Microscópicamente tiene el 90 % de los alveolos ocupados por
hemorragia intraalveolar con hematíes extravasados en las
luces alveolares. No se reconoce exudado fibrinoleucocitario.
Además se observan macrófagos con hemosiderina que indican
una hemorragia pulmonar antigua. Acompañando estas lesiones,
se evidencian membranas hialinas e hiperplasia de neumocitos
tipo 2, correspondiendo a daño alveolar difuso, en etapa
exudativa y proliferativa, que indica por o menos 7 días de
evolución (figura 3). Se reconoce un infarto hemorrágico en
pulmón derecho con microtrombosis que corresponde a la
presencia de trombos hialinos en los pequeños vasos
sanguíneos.
|
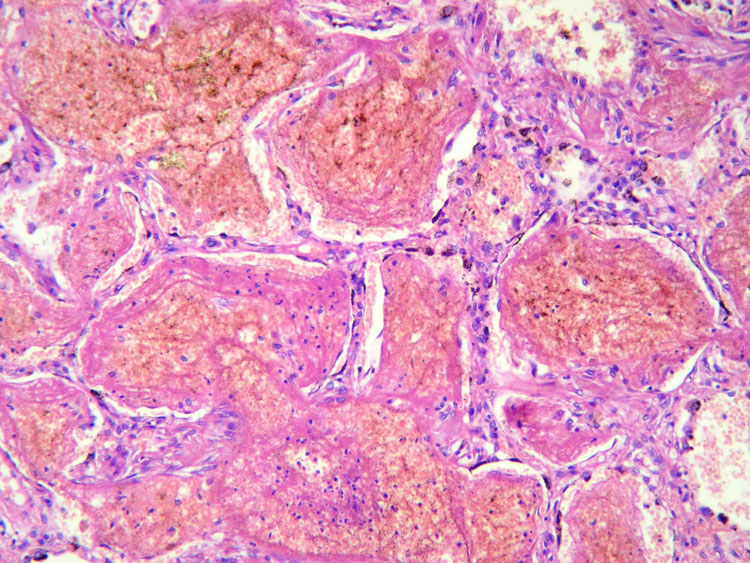 |
Figura 3: Autopsia: Pulmón con
daño alveolar difuso y hemorragia intraalveolar
(H/E)
|
Dentro del cuadro evolutivo, se observan áreas de BOOP,
correspondientes a tapones fibroblásticos que ocupan las
luces de los alveolos y bronquiolos terminales y que están
constituidas por tejido fibroconectivo o fibroblastos que
empiezan a proliferar y a depositar colágeno (figura 4).
Dicha lesión es vinculable a GVH por ser un transplantado de
médula ósea, pero es un término inespecífico porque puede
vincularse a efectos por drogas, infecciones o distress.
|
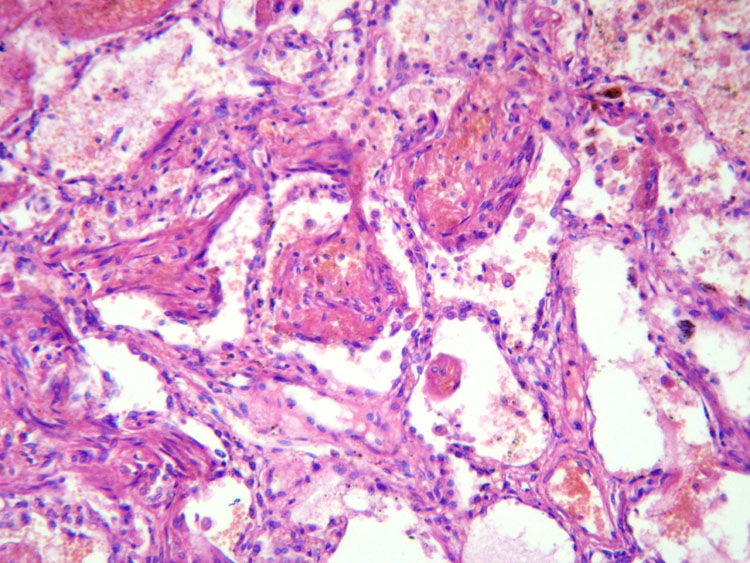 |
Figura 4:
Autopsia: Pulmón con BOOP (H/E)
|
Además, tiene en la luz bronquial de los bronquios y
bronquiolos moco con fibrina, polimorfonucleares neutrófilos
y hemorragia.
No encontramos efecto citopático viral ni signos de
aspergilosis. .
También tiene fibrosis subpleural e intersticial, resaltada
con la técnica de Masson y fibrosis perivascular, vinculable
a efecto de drogas y quimioterapia.
A
nivel cardíaco, el corazón tiene un peso de 440 grs. El
pericardio no presenta lesiones a destacar. A la apertura de
las cavidades, el ventrículo izquierdo mide 22 mm de
diámetro, hipertrófico, con válvulas sin lesiones. El
ventrículo derecho tiene una pared de 11 mm de diámetro. Las
arterias coronarias se ven permeables sin lesiones.
Microscópicamente en ambos ventrículos se observan fibras
miocárdicas onduladas, con pérdida de estriaciones y un
incipiente infiltrado inflamatorio, vinculables a isquemia
miocárdica de 3 a 6 horas. Tiene signos de hipertrofia
muscular, fibrosis subendocárdica e hipertrofia vascular
que, en este caso, pueden vincularse como efectos
secundarios a drogas.
Los ganglios mediastinales tienen signos de antracosis pero
llama la atención la depleción linfocitaria de los mismos.
La médula ósea, correspondiente a un fragmento de costilla,
donde sólo se observa freno en la maduración hematopoyética
pero no recaída de su enfermedad.
Finalmente, los diagnósticos son los siguientes:
-
Compromiso
del 90% de los alvéolos pulmonares.
-
Hemorragia intraalveolar difusa
reciente con hemorragia antigua focal.
-
Daño
alveolar difuso. Etapas I y II.
-
Infarto
pulmonar derecho con microtrombosis bilateral.
-
Bronquitis
aguda focal.
-
BOOP.
-
Fibrosis
subpleural e intersticial.
-
Isquemia
miocárdica incipiente.
-
Cardiomegalia
con hipertrofia biventricular.
-
Fibrosis
subendocárdica. Hipertrofia vascular.
-
Depleción
linfocitaria de ganglio linfáticos mediastinales.
-
Freno
en la maduración en médula ósea.
-
Esofagitis
crónica moderada.

|