TRABAJO ORIGINAL
Accidente cerebrovascular.
¿existen diferencias en la funcion sistolica de la orejuela
de la auricula izquierda entre pacientes con y sin foramen
oval permeable?
Stroke. are
there any difference between patients with or without patent
foramen ovale in left atrial appendage systolic function?
Alejandro E. Contreras1, Federico Perrote2, Ignacio
Concari2, Eduardo J. Brenna1, Cecilia Lucero2
Revista Facultad de Ciencias
Medicas 2012; 69(4):197-201
1-Servicio de Cardiología.
Hospital Privado Centro Médico de Córdoba. Córdoba.
Argentina.
2-Servicio de Neurología . Hospital Privado Centro Médico de
Córdoba. Córdoba. Argentina.
Correspondencia: Alejandro
Contreras. Hospital Privado Centro Médico de Córdoba.
Naciones Unidas 346. Bº Parque Velez Sarfield. CP 5016.
Córdoba. Argentina. TE: 543514688220. FAX: 543514688818.
E-mail:
aletreras@hotmail.com
Introducción
El foramen oval permeable (FOP) es un factor de riesgo menor
de eventos cerebrovasculares isquémicos, debido a embolia
paradojal proveniente de la circulación venosa1; Sin
embargo, el único estudio randomizado hasta el momento, que
comparó tratamiento médico con cierre percutáneo del FOP,
demostró que el cierre con dispositivo no aporta beneficios
en recurrencia de ACV o crisis isquémicas transitorias (CIT)
2.
El deterioro de la función de la orejuela de la aurícula
izquierda (OAI), detectada por ecocardiografía
transesofágica (ETE), es un predictor importante de
tromboembolismo, tanto en pacientes con fibrilación
auricular como en pacientes con ritmo sinusal3,4.
El objetivo del presente trabajo fue evaluar la función
sistólica de la OAI en un grupo de pacientes con eventos
cerebrovasculares isquémicos y comparar dicha función entre
pacientes con y sin FOP.
Material y métodos
Entre septiembre de 2010 y octubre de 2011, un total de
30 pacientes fueron enviados al departamento de
ecocardiografía para descartar fuente de cardioembolia, en
pacientes con ACV/CIT. Los pacientes fueron evaluados por 2
neurólogos y fueron excluidos aquellos pacientes en los que
no se contaba con imágenes cerebrales (tomografía o
resonancia magnética) que certificara el evento isquémico
(n= 13).
En definitiva fueron 17 pacientes que cumplieron con los
siguientes criterios de inclusión:
1) presencia de ritmo
sinusal,
2) fracción de eyección del ventrículo izquierdo (VI)
igual o mayor a 50%,
3) ausencia de anormalidades en la
motilidad regional del VI,
4) ausencia de trombos en la
orejuela de la aurícula izquierda
5) ausencia de
enfermedad ateroesclerótica carotidea.
Ecocardiograma
Se realizó un ecocardiograma transtorácico (GE Vivid S5) de
acuerdo a las recomendaciones de American Society of
Echocardiography, que incluyó modo M, bidimensional y
evaluación de flujos con Doppler.
A todos los pacientes se les realizó un ecocardiograma
transesofágico (sonda multiplanar 6-Mhz, 6Tc). Se requería
ayuno de 8 horas y recibieron anestesia faríngea con
lidocaína tópica al 10%. Si era necesario la sedación, se
usaba midazolam endovenoso. Se obtenía una vía venosa
periférica en miembro superior derecho y con llave de 3 vías
se inyectaba solución salina agitada para evaluación de
shunt de derecha a izquierda a través de foramen oval. Se
definía al foramen oval permeable cuando había pasaje de
burbujas de derecha a izquierda en los primeros 3 latidos
luego del relleno con contraste de la aurícula derecha.
Además se realizaba maniobra de Valsalva y se evaluaba el
pasaje de burbujas en el periodo de relajación de dicha
maniobra.
Se definió foramen oval permeable al pasaje de al menos una
burbuja, siendo FOP pequeño cuando dicho pasaje era menor a
20 o FOP grande cuando era mayor a 20 burbujas. El aneurisma
del septum interauricular fue definido como la excursión del
mismo, mayor a 10 mm, desde la posición original hacia la
izquierda o derecha.
La OAI fue visualizada en la vista medioesofágica, con
rotación del transductor entre 0 y 180 grados. Se descartaba
la presencia de trombos y se evaluaban las velocidades de
flujo en OAI con Doppler pulsado, posicionando el volumen de
muestra en el tercio proximal de la OAI. Se media el pico de
velocidad de la onda de contracción (vaciado) de OAI,
inmediatamente posterior a la onda P del electrocardiograma
(figura 1). Fueron promediadas las velocidades de 3 latidos
consecutivos.
Figura
1. Ecocardiograma transesofágico. Velocidad sistólica de
orejuela auricular izquierda con Doppler pulsado.
Análisis estadístico
Todos los análisis estadísticos fueron realizados con SPSS
versión 15. Las variables categóricas se presentan como
porcentajes y las variables continuas como promedio o
mediana y desviación estándar. Para la comparación de las
velocidades sistólicas de OAI se usó test T para muestras
independientes. Un grupo control compuesto por pacientes
evaluados con ETE por padecer migrañas fue usado para
comparar las velocidades sistólicas de la OAI con los
pacientes con eventos isquémicos. Un valor de p menor a 0,05
fue considerado significativo.
Resultados
Se incluyeron 17 pacientes, 8 mujeres y 9 hombres, con una
edad media de 54,1 ± 19,5 años y 8 pacientes tenían menos de
55 años de edad. En la tabla 1 se describen las
características basales de la población. Todos los pacientes
habían sufrido un evento cerebrovascular isquémico
criptogénico, el 41,2% habían tenido ACV, el 52,9% CIT y el
5,9% amaurosis fugaz. El ETE fue realizado 110 días (rango
1-1055 días) posterior al evento isquémico.
En la evaluación con ETE, el 11,8% tuvo aneurisma del septum
interauricular y el 35,3% foramen oval permeable. El 29,4%
tenía ateromatosis aortica leve (no debris) en raíz aortica
o aorta torácica ascendente o descendente. La velocidad
sistólica media de la OAI fue 66,3 ± 20,3 cm/seg. No hubo
diferencia en la velocidad sistólica de la OAI entre
pacientes con o sin FOP (67,5 ± 11,8 cm/seg vs 65,7 ± 24,3
cm/seg respectivamente, p= 0,87). En la Tabla 2 se comparan
las variables clínicas entre pacientes con y sin FOP. El
grupo control compuesto por 8 pacientes, 5 mujeres y 3
hombres, con una edad media de 39,5 ± 18 años, de los cuales
3 tuvieron FOP (37,5%), la velocidad sistólica de la OAI fue
de 77,6 ± 28,9 cm/seg, sin diferencias significativas con
los pacientes isquémicos (figura 2).
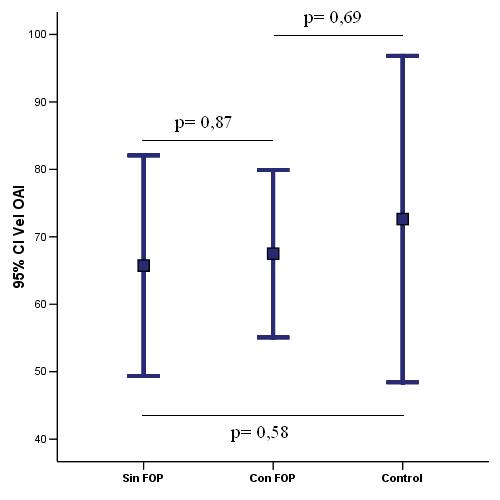  |
Figura
2. Velocidades sistólicas en la orejuela auricular izquierda
(OAI) en cm/seg. Comparación entre pacientes con y sin
foramen oval permeable (FOP) y grupo control.
 |
 |
|
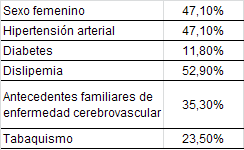
Tabla 1. Características generales |
Tabla 2.
Comparación entre pacientes con y sin foramen oval
permeable (FOP). Hipertensión arterial (HTA). |
Discusión
La asociación entre la persistencia del FOP y el ACV fue
descripta por primera vez en el año 1988, en pacientes
jóvenes, en estudios de casos y controles5,6. El
mecanismo fisiopatológico que explicaría esta asociación es
la embolia paradojal, sin embargo, la detección del embolo
transcurriendo a través del FOP, se ha detectado en pocas
ocasiones y a menudo es un mecanismo presuntivo más que una
certeza.
Existen dudas sobre el rol del FOP en el ACV criptogénico,
ya que en 2 estudios poblacionales de pacientes sin ACV
previo, con seguimientos mayores a 5 años, el FOP no resultó
ser un predictor de riesgo independiente de eventos
cerebrovasculares7,8. El único estudio randomizado
publicado hasta el momento, comparando el cierre percutáneo
del FOP vs tratamiento médico, en pacientes menores de 60
años, con ACV criptogénico, mostró tasas similares de
recurrencias de eventos cerebrovasculares, incrementando las
dudas acerca del papel fisiopatológico del FOP2.
Posibles factores asociados al FOP podrían incrementar el
riesgo de eventos cardiovasculares, de los cuales el más
relevante es la presencia de aneurisma del septum
interauricular. En un meta análisis, el FOP incrementó el
riesgo de ACV 1,83 veces y cuando se asocia a ASA el riesgo
se incrementa a 5 veces9. Otros factores asociados
implicados en el incremento de riesgo del FOP son:
1) El
tamaño del túnel (separación entre el septum primun y
secundum) y la cantidad de burbujas que pasan a la aurícula
izquierda10-12.
2) Presencia de trombosis venosa profunda
concomitante13.
3) Estados de hipercoagulabilidad
concomitantes.
La OAI es el lugar donde comúnmente se forman los trombos,
en pacientes con fibrilación auricular. En estudios previos,
el deterioro de la función de la OAI se ha asociado a la
formación de trombos14. En la práctica diaria, la
evaluación de la función sistólica de la OAI, puede ser de
gran ayuda para el diagnóstico diferencial de masas dentro
del apéndice auricular, descartando la presencia de trombos
cuando dicha función es normal15.
El ritmo cardíaco es un determinante en la función sistólica
de la OAI, existiendo diferencias significativas entre
pacientes con ritmo sinusal y fibrilación auricular. Handke
y col. demostraron que también hay diferencias entre
pacientes con ritmo sinusal al momento del ETE, dependiendo
si hubo o no fibrilación auricular paroxística.
Independientemente del ritmo hallado, encontraron que una
velocidad menor a 55 cm/seg, fue un predictor de formación
de trombos o contraste espontaneo en la OAI16. Ozer y col
describieron en pacientes con ACV que las velocidades en la
OAI están disminuidas tanto en pacientes en ritmo sinusal
como con fibrilación auricular en casos de ACV
cardioembólico17.
En nuestro trabajo, no encontramos diferencias en la función
del apéndice auricular entre pacientes con o sin FOP,
quienes habían sufrido ACV. Todos nuestros pacientes estaban
en ritmo sinusal y no tenían historia previa de fibrilación
auricular. La velocidad sistólica de la OAI fue normal en
ambos grupos (con y sin FOP) y en el grupo control. Ningún
paciente en el grupo con FOP tuvo velocidades menores a 55
cm/seg.
Rigatelli y col., en un grupo de 98 pacientes con eventos
embólicos (57% con migrañas), no encontraron diferencias en
la función de la OAI entre pacientes con y sin FOP, en
cambio, observaron diferencias en la función de la auricula
izquierda, con fisiologia similar a pacientes con
fibrilación auricular en aquellos que tenían FOP18.
Conclusión
En pacientes con ACV/CIT y FOP, la función sistólica del
apendice auricular evaluada con Doppler pulsado por
ecografia transesofágica es similar a los controles sanos y
a pacientes con ACV y sin FOP. El apendice auricular en
pacientes con FOP no parece tener un papel importante en la
fisiopatología del accidente cerebrovascular.
Referencias
1. Pepi M, Evangelista A, Nihoyannopoulos P, Flachskampf FA,
Athanassopoulos G, Colonna P, Habib G, Ringelstein B, Sicari
R, Zamorano J. Recommendations for echocardiography use in
the diagnosis and management of cardiac sources of embolism.
Eur J Echocardiography 2010;11:461-76
PubMed
2. Furlan AJ, Reisman N, Massaro J, Mauri L, Adams H, Albers
GW, Felberg R, Herrmann H, Kar S, Landzberg M, Raizner A,
Wechsler L. Closure or medical therapy for cryptogenic
stroke with patent foramen ovale. N Engl J Med 2012, 366:
991-9
Full Text
3. Agmon Y, Khandheria B, Gentile F, Seward JB.
Echocardiographic assessment of the left atrial appendage. J
Am Coll Cardiol 1999;34:1867-77
PubMed
4. Tuluce SY, Kayikcioglu M, Tuluce K, Yilmaz MG, Ozdogan O,
Aydin M, Hasdemir C. Assessment of left atrial appendage
function during sinus rhythm in patients with hypertrophic
cardiomyopaty: Transesophageal echocardiography and tissue
Doppler study. J Am Soc Echocardiogr 2010;23:1207-16
PubMed
5. Lechat P, Mas JL, Lascault G, Loron P, Theard M, Klimczac
M, Drobinski G, Thomas D, Grosgogeat Y. Prevalence of patent
foramen ovale in patients with stroke. N Engl J Med
1988;318:1148-52
PubMed
6. Webster MW, Chancellor AM, Smith HJ, Swift DL, Sharpe DN,
Bass NM, Glasgow GL. Patent foramen ovale in young stroke
patients. Lancet 1988;2:11-2
Lancet
7. Meissner I, Khandheria BK, Heit JA, Petty GW, Sheps SG,
Schwartz GL, Whisnant JP, Wiebers DO, Covalt JL, Petterson
TM, Christianson TJ, Agmon Y. Patent foramen ovale: innocent
or guilty? Evidence from a prospective population-based
study. J Am Coll Cardiol 2006;47:440-5
PubMed
8. Di Tullio MR, Sacco RL, Sciacca RR, Jin Z, Homma S.
Patent foramen ovale and the risk of ischemic stroke in a
multiethnic population. J Am Coll Cardiol 2007;49:797-802
PubMed
9. Overell JR, Bone I, Lees KR. Interatrial septal
abnormalities and stroke: a meta-analysis of case-control
studies. Neurology 2000;55:1172-9
PubMed
10. Lee JY, Song JK, Song JM, Kang DH, Yun SC, Kang DW, Kwon
SU, Kim JS. Association between anatomic features of atrial
septal abnormalities obtained by Omni-Plane transesophageal
echocardiography and stroke recurrence in cryptogenic stroke
patients with patent foramen ovale. Am J Cardiol
2010;106:129-34
PubMed
11. Fazio G, Ferro G, Carita P, Lunetta M, Gullotti A,
Trapani R, Fabbiano A, Novo G, Novo S. The PFO anatomy
evaluation as possible tool to stratify the associated risks
and the benefits arising from the closure. Eur J
Echocardiography 2010;11:488-91
PubMed
12. Telman G, Yalonetsky S, Kouperberg E, Sprecher E, Lorber
A, Yarnitsky D. Size of PFO and amount of microembolic
signals in patients with ischaemic stroke or TIA. Eur J
Neurol 2008;15:969-72
PubMed
13. Stollberger C, Slany J, Schuster I, Leitner H, Winkler
WB, Karnik R. The prevalence of deep venous thrombosis in
patients with suspected paradoxical embolism. Ann Intern Med
1993;119:461-5
PubMed
14. Fatkin D, Kelly RP, Feneley MP. Relation between left
atrial appendage blood flow velocity, spontaneous
echocardiographic contrast and thromboembolic risk in vivo.
J Am Coll Cardiol 1994;23:961-9
PubMed
15. Seward JB, Khandheria BK, Oh JK, Freeman WK, Tajik AJ.
Critical appraisal of transesophageal echocardiography:
limitations, pitfalls, and complications. J Am Soc
Echocardiogr 1992;5:288-305
PubMed
16. Handke M, Harloff A, Hetzel A, Olschewski M, Bode C,
Geibel A. Left atrial appendage flow velocity as a
quantitative surrogate parameter for thromboembolic risk:
determinants and relationship to spontaneous echocontrast
and thrombus formation- A transesophageal echocardiography
study in 500 patients with cerebral ischemia. J Am Soc
Echocardiogr 2005;18:1266-72
PubMed
17. Ozer N, Tokgozoglu L, Ovunc K, Kabakc K, Aksoyec S,
Aytemir K. Left atrial appendage function in patients with
cardioembolic stroke in sinus rhythm and atrial
fibrillation. J Am Soc Echocardiogr 2000;13:661-5
PubMed
18. Rigatelli G, Aggio S, Cardaioli P, Braggion G, Giordan
M, Dell’avvocata F, Chinaglia M, Rigatelli G, Roncon L, Chen
JP. Left atrial dysfunction in patients with patent foramen
ovale and atrial septal aneurysm: An alternative concurrent
mechanism for arterial embolism?. J Am Coll Cardiol Intv
2009;2;655-62
PubMed
|